
La leucemia aguda pediátrica es el cáncer más frecuente en México, representando cerca del 65 % de los casos en niños. Su agresividad compromete rápidamente la médula ósea, generando neutropenia y un estado de inmunosupresión profunda que convierte al paciente en altamente vulnerable a infecciones oportunistas.
En entrevista, Rodrigo Chablé, licenciado en Químico Farmacéutico Biólogo y maestro en Ciencias Bioquímicas por la Universidad Autónoma de Yucatán (UADY), explica que su formación se ha enfocado específicamente en diagnóstico molecular y celular:

“Mi formación se enfoca en el diagnóstico molecular y celular, específicamente en técnicas de biología molecular como PCR, secuenciación y citometría de flujo en el linaje linfoide”.
Su trayectoria combina biología molecular, análisis celular avanzado y estandarización de procesos diagnósticos en instituciones públicas. Actualmente participa en la implementación de tecnologías de diagnóstico de última generación, buscando elevar la calidad diagnóstica bajo estándares internacionales.
Como él mismo señala:
“Se está implementando esta técnica para que se pueda proporcionar en una institución de origen público. El trabajo va aunado a que los nuevos usuarios la puedan implementar de una manera exitosa y consciente para mejorar la calidad de los diagnósticos”.
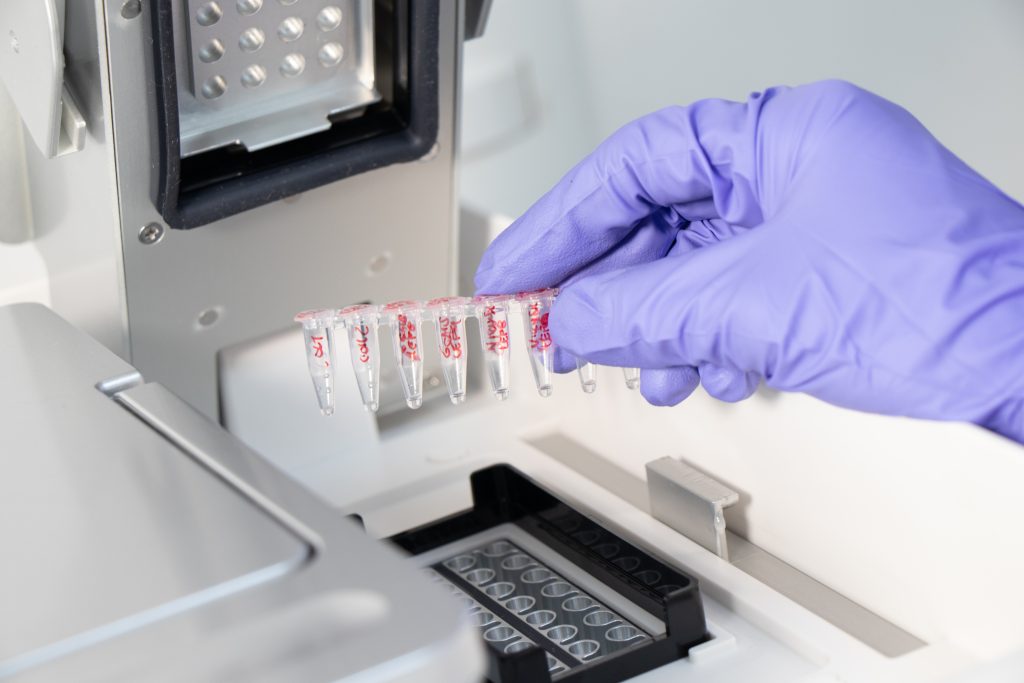
Este enfoque no solo implica tecnología, sino capacitación, transferencia de conocimiento y consolidación de procesos hospitalarios.

La citometría de flujo multiparamétrica constituye hoy el estándar para la clasificación de leucemias agudas. Permite identificar el linaje celular y los perfiles inmunológicos de las células neoplásicas a partir de una muestra de médula ósea.
Rodrigo Chablé enfatiza su impacto clínico:
“La citometría de flujo ha sido fundamental en el diagnóstico, clasificación y seguimiento de neoplasias hematológicas”.
Uno de los avances más relevantes dentro del proyecto integral ha sido la reducción en los tiempos diagnósticos:
“Antes podíamos tardar entre siete y diez días; ahora podemos tener un resultado prácticamente al día siguiente”.
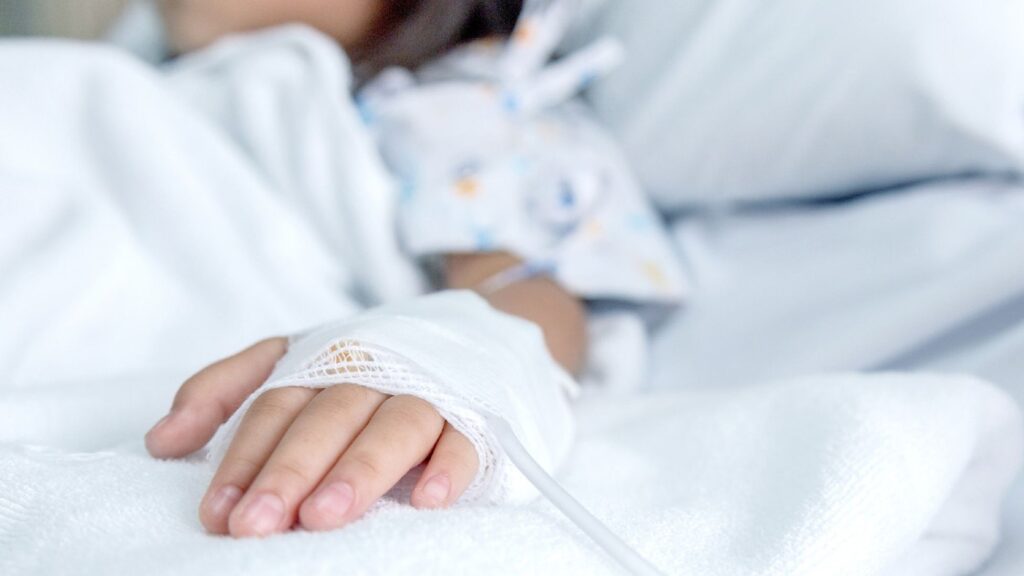
En patologías como la leucemia aguda, esta diferencia temporal puede definir el inicio temprano de quimioterapia dirigida.
Además, la implementación bajo protocolos estandarizados internacionalmente permite resultados comparables con centros de alta especialidad:
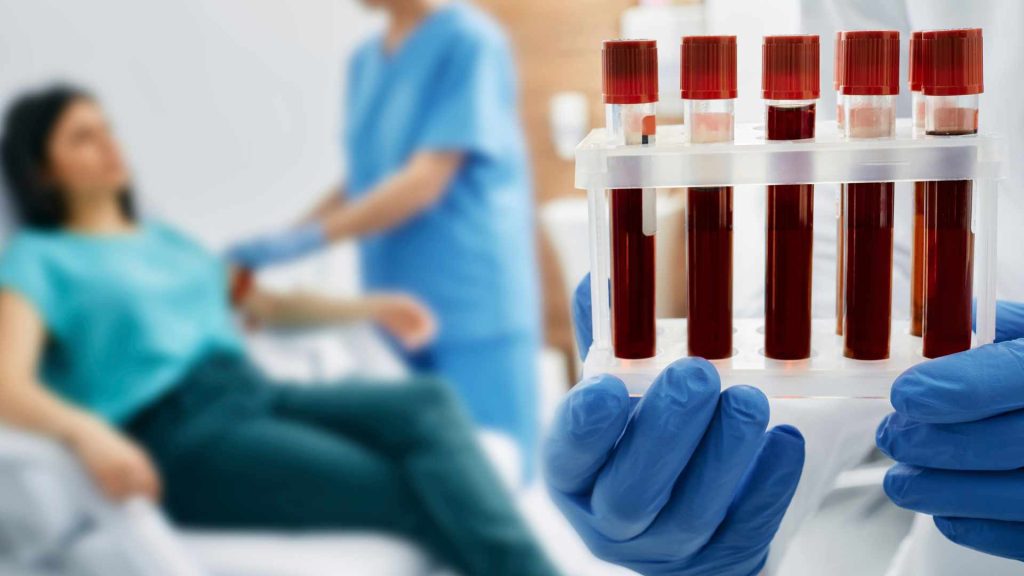
“Trabajamos con protocolos que hacen el diagnóstico reproducible con cualquier hospital de primer mundo”.
Esto posiciona al sistema público dentro de una red de calidad diagnóstica global.

La Leucopenia secundaria a leucemia y quimioterapia convierte a los pacientes pediátricos en extremadamente vulnerables.
Chablé lo resume con claridad:
“La leucemia desplaza la producción normal en médula ósea; el paciente queda prácticamente sin defensas. En ese momento, cualquier infección puede volverse grave en cuestión de horas”.
El reto clínico es doble: diagnosticar el cáncer con precisión y, al mismo tiempo, identificar de manera rápida cualquier agente infeccioso.
“Cuando el paciente presenta síntomas es porque ya la enfermedad está en un estado avanzado. Identificar tanto la leucemia como cualquier infección es completamente necesario para iniciar tratamiento oportuno”.

Para enfrentar el riesgo infeccioso en inmunocomprometidos, el proyecto incorpora espectrometría de masas MALDI-TOF, una tecnología que identifica microorganismos mediante su perfil proteico.
Según Chablé:
“En 30 minutos ya tienes el diagnóstico”.
Este tiempo contrasta con los métodos tradicionales basados en reacciones metabólicas, dependientes de cultivos y crecimiento de colonias de microorganismos, que pueden tardar entre 24 y 48 horas. En un paciente con leucopenia febril, esa diferencia puede ser determinante.
Además, el especialista destaca un beneficio operativo:
“La tecnología permite que incluso personal en formación pueda identificar microorganismos con alta precisión, algo que antes dependía mucho de la experiencia”.
La estandarización tecnológica reduce la variabilidad y mejora la toma de decisiones terapéuticas, además de contribuir al uso racional de antibióticos.

Más allá de la incorporación de equipos, el proyecto representa un modelo integral de diagnóstico que articula hematología, microbiología y procesos hospitalarios.
Rodrigo Chablé subraya que el objetivo no es únicamente tecnológico:
“No se trata solo de tener la tecnología, sino de que se implemente de manera consciente en la rutina diaria del hospital”.
La transferencia de conocimiento a “nuevos usuarios” garantiza sostenibilidad del modelo y mejora continua en la calidad diagnóstica.
Finalmente, el especialista concluye:
“Reducir el tiempo diagnóstico cambia el pronóstico. Dar un diagnóstico rápido se vuelve crucial”.
La integración de citometría de flujo multiparamétrica y MALDI-TOF dentro de un proyecto estructurado de diagnóstico oncohematológico y microbiológico eleva el estándar del sistema público hacia un nivel comparable con centros internacionales.
El caso presentado por Rodrigo Chablé demuestra que la innovación diagnóstica no depende exclusivamente de la tecnología, sino de su implementación estratégica, estandarizada y formativa.
En pacientes inmunocomprometidos, donde cada hora es decisiva, la precisión y la rapidez no son ventajas competitivas: son condiciones para salvar vidas.

